 “Scambierebbe il suo detersivo XYZ con due fustini di un detersivo qualunque?”.
“Scambierebbe il suo detersivo XYZ con due fustini di un detersivo qualunque?”.
Questo tormentone pubblicitario ci ha accompagnato per molti anni a testimonianza di una corsa al miglioramento di un prodotto che sempre di più è diventato l’icona del mondo moderno, pulito e sempre più distante dall’ambiente naturale.
L’immagine sulla destra ci dà un’idea della proliferazione di sostanze pensate per eliminare lo sporco nelle più svariate situazioni. Ma cosa differenzia e cosa accomuna tutti questi prodotti? E come ci si è arrivati?
Per pulire qualcosa bisogna sporcarne un’altra. Se la cosa che si sporca è l’acqua, essa può essere rimossa insieme allo sporco e lo scopo sarà stato raggiunto.
Il problema quindi diventa: come possiamo fare in modo che la maggior quantità di sporco possibile venga disciolto, o al massimo inglobato, nella massa d’acqua?
Ci sono principalmente due ostacoli da superare: uno è la tensione superficiale dell’acqua stessa, a causa della quale l’acqua può non bagnare affatto la superficie che si vuole lavare. E l’altra è la non solubilità delle sostanze grasse, che tendono a rimanere aggregate fra di loro e ben separate dall’acqua con cui vorremmo che andassero via.
 La tensione superficiale è quel fenomeno fisico per cui le molecole che si trovano sulla superficie di un fluido, all’interfaccia con un’altra sostanza, solida o gassosa, tendono a rimanere coese con la massa liquida formando una sorta di pellicola che ne impedisce la dispersione. Non si tratta di una vera e propria pellicola, ma di un accumulo di energia potenziale che mantiene le molecole legate le une alle altre.
La tensione superficiale è quel fenomeno fisico per cui le molecole che si trovano sulla superficie di un fluido, all’interfaccia con un’altra sostanza, solida o gassosa, tendono a rimanere coese con la massa liquida formando una sorta di pellicola che ne impedisce la dispersione. Non si tratta di una vera e propria pellicola, ma di un accumulo di energia potenziale che mantiene le molecole legate le une alle altre.
Il risultato è che per rompere la superficie di un liquido è necessaria una certa forza e di questo si avvantaggiano per esempio gli insetti che sono sufficientemente leggeri da poter camminare sulla superficie acquatica di laghi e fiumi. Con un po’ di attenzione possiamo appoggiare anche piccoli oggetti, come monetine, graffette, spilli, ecc. sul pelo dell’acqua contenuta in un bicchiere senza che essi affondino.
Quindi il primo compito di un detergente in generale è quello di diminuire la tensione superficiale. L’acqua deve poter aderire facilmente a qualsiasi superficie, infiltrarsi in ogni fessura, per poter bagnare l’oggetto e raggiungere lo sporco.
Il principale componente di un detersivo è quindi un tensioattivo. Cioè una sostanza in grado di modificare la tensione superficiale dell’acqua in cui la sciogliamo. Il tensioattivo permette all’acqua anche di attaccarsi allo sporco grasso e oleoso che spesso è quello di cui maggiormente vogliamo disfarci, essendo terreno di coltura per microorganismi di ogni genere.
Il meccanismo di azione di un tensioattivo è dovuto alla particolare caratteristica delle molecole che lo compongono. Si tratta normalmente di molecole organiche lineari in cui si individua una “coda” lipofila, cioè che presentà affinità con i grassi, e una “testa” idrofila, cioè che presenta affinità con l’acqua.
Quando introduciamo un tensioattivo nell’acqua questo si lega allo sporco grasso tramite le sue code idrofobe mentre le teste vengono attratte verso la massa acquosa, col risultato che le particelle di grasso vengono inglobate all’interno di una specie di bolla la cui superficie è costituita dalle teste idrofile. Queste particelle sono libere di moversi nel fluido e con esso rimosse.
L’immagine seguente schematizza il processo sopra descritto.
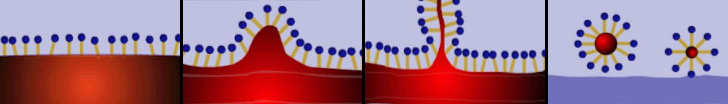
Nei detergenti moderni ai tensioattivi si affiancano diverse altre sostanze che aiutano il composto a specializzarsi nella rimozione di particolari tipi di sporco. Ne vedremo qualcuna nei paragrafi seguenti.
 -0
-0  )
)

10 Aprile 2020 at 15:39
Ciao sono Aldo da Albania come funziona per compra dedersivo da voi per ingreso a paeze mioa
10 Aprile 2020 at 16:56
Ciao Aldo,
mi spiace. Questo non è un sito di e-commerce.
Sei comunque il benvenuto se vuoi continuare la lettura degli articoli.